更新日:2025年5月15日
治験に関するお知らせ
治験審査委員会
| 名称 | 愛媛県立中央病院治験審査委員会 |
|---|---|
| 設置者 | 愛媛県立中央病院長 |
| 所在地 | 愛媛県松山市春日町83番地 |
| 委員数 | 21名 |
| 委員名簿 | 治験審査委員会委員名簿(2025年5月1日) |
| 設置要綱 | 治験審査委員会設置要綱 |
| 開催状況 |
年9回(4・8・11月は原則休会) |
| 会議の記録の概要 |
※今年度分は、治験事務局で保管しています。 |
治験依頼者の方へ
当院では、健康な方を対象とした治験は実施しておりません。治験コーディネーター業務および事務局業務(一部)は、治験施設支援機関(SMO)に委託しています。
実施体制
病院の実施体制をご覧ください。
治験実施までの流れ
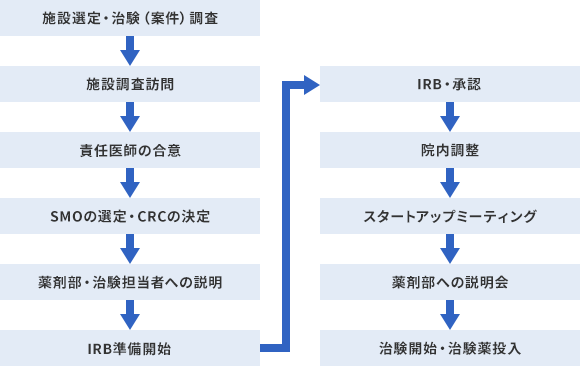
治験等依頼の手続き・問い合わせ窓口
治験責任医師と治験実施計画書について合意後、必要な書類を提出してください。
申請資料の締め切りは、原則として委員会開催日の3週間前となります。
〒790-0024 愛媛県松山市春日町83番地
愛媛県立中央病院 総務医事課 庶務係内 治験事務局
電話番号:089-947-1111(内線5524)
メールアドレス:c-volunteer★eph.pref.ehime.jp (★を@にご変換ください)
手順書(SOP)・様式等
- 当院では、統一書式を採用しています。
統一書式は「公益社団法人日本医師会 治験促進センター」より入手をお願いします。
その他の病院様式は下記よりダウンロードしてください。
経費について
2016年9月IRB新規案件より、実績に基づく支払い(マイルストーン方式)を導入することといたしました。算出方法等につきましては、「愛媛県立中央病院 受託研究費等の算定内規」をご覧ください。
治験の実績等
実施中の治験等(2024年4月1日現在)
| 診療科名 | 対象疾患 | 治験段階 | 備考 |
|---|---|---|---|
| 循環器内科 | 心房細動 | 第Ⅲ相 | |
| 消化器内科 | 潰瘍性大腸炎 | 第Ⅱ/Ⅲ相 | |
| 潰瘍性大腸炎(2件) | 第Ⅲ相 | ||
| 肝細胞がん | 第Ⅰ/Ⅱ相 | ||
| 肝細胞がん(5件) | 第Ⅲ相 | ||
| 血液内科 | 温式自己免疫性溶血性貧血 | 第Ⅲ相 | |
| 急性骨髄性白血病 | 第Ⅲ相 | ||
| 多発性骨髄腫 | 第Ⅲ相 | ||
| 呼吸器内科 | 好酸球性重症喘息 | 第Ⅲ相 | |
| 脳神経内科 | 自己免疫性脳炎 | 第Ⅲ相 | |
| 糖尿病・内分泌内科 | 2型糖尿病 | 第Ⅲ相 | |
| 耳鼻咽喉科・頭頚部外科 | 慢性副鼻腔炎 | 第Ⅲ相 | |
| 整形外科 | 急性期脊髄損傷 | 第Ⅰ/Ⅱ相 |
年度別新規治験等の受託件数
| 年度 | 医薬品 | 受託件数 | 医師主導 治験 |
||||||
|---|---|---|---|---|---|---|---|---|---|
| 第Ⅰ相 | 第Ⅱ相 | 第Ⅲ相 | 第Ⅳ相 | 製造販売後 臨床試験 |
人道的見地から実施される治験 | その他 | |||
| 2016年度 | 6 | 1 | 1 | 8 | |||||
| 2017年度 | 4 | 13 | 1 | 18 | |||||
| 2018年度 | 8 | 8 | |||||||
| 2019年度 | 3 | 7 | 1 | 11 | |||||
| 2020年度 | 2 | 1 | 3 | ||||||
| 2021年度 | 1 | 3 | 4 | ||||||
| 2022年度 | 1 | 2 | 3 | ||||||
| 2023年度 | 1 | 8 | 9 | 1 | |||||
診療科別新規治験等の受託件数
| 診療科名 | 2016 | 2017 | 2018 | 2019 | 2020 | 2021 | 2022 | 2023 | |
|---|---|---|---|---|---|---|---|---|---|
| 治験 | 治験 | 治験 | 治験 | 治験 | 治験 | 治験 | 治験 | 医師主導治験 | |
| 消化器内科 | 1 | 4 | 2 | 6 | 3 | 1 | 4 | ||
| 呼吸器内科 | 1 | 2 | |||||||
| 循環器内科 | 1 | 3 | 2 | 1 | 1 | ||||
| 腎臓内科 | 3 | 6 | 2 | ||||||
| 糖尿病・ 内分泌内科 |
1 | ||||||||
| 血液内科 | 4 | 2 | 1 | 1 | 3 | 1 | |||
| 脳神経内科 | 1 | 1 | |||||||
| 小児科 | |||||||||
| 心臓血管外科 | 1 | ||||||||
| 消化器外科 | 1 | ||||||||
| 産婦人科 | |||||||||
| 眼科 | 1 | ||||||||
| 脳神経外科 | 1 | ||||||||
| 整形外科 | 1 | 1 | |||||||
| 耳鼻咽喉科・頭頚部外科 | 1 | ||||||||
| 計 | 8 | 18 | 8 | 11 | 3 | 4 | 3 | 9 | 1 |
募集中治験等(2024年4月1日現在)
| 診療科名 | 対象疾患 | 治験薬名 (または治験薬コード) |
治験段階 | 備考 |
|---|---|---|---|---|
| 消化器内科 | 肝細胞がん | デュルバルマブ・トレメリムマブ | 第Ⅲ相 | |
| 肝細胞がん | アテゾリズマブ・ベバシズマブ・チラゴルマブ | 第Ⅲ相 | ||
| 潰瘍性大腸炎 | ABX464 | 第Ⅲ相 | ||
| 呼吸器内科 | 好酸球性重症喘息 | GSK3511294 | 第Ⅲ相 | |
| 血液内科 |
温式自己免疫性溶血性貧血 |
VAY736 | 第Ⅲ相 | |
|
急性骨髄性白血病 |
KRP203 | 第Ⅲ相 | ||
|
多発性骨髄腫 |
エルラナタマブ | 第Ⅲ相 | ||
| 脳神経内科 | 自己免疫性脳炎 | NPB-01 | 第Ⅲ相 | |
| 循環器内科 | 心房細動 | Milvexian | 第Ⅲ相 | |
| 整形外科 | 急性期脊髄損傷 | KA-301 | 第Ⅰ/Ⅱ相 |
※詳細は主治医を通じてお問い合わせください。


